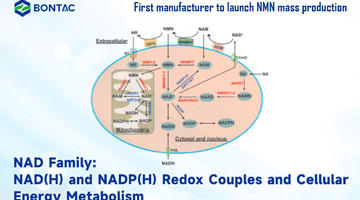
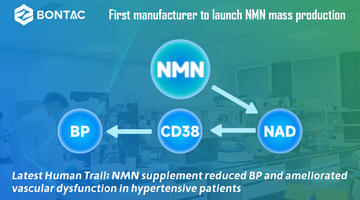
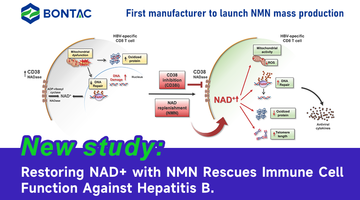
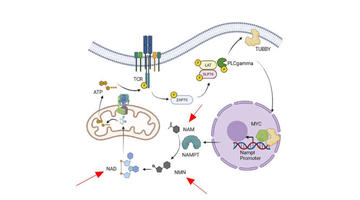
Politica di supervisione per NMN in Giappone, Cina, America, Australia e Canada
Politiche di supervisione per NMN in Giappone, Cina, America, Australia e Canada
Le ricerche mainstream di NMN sono state condotte da un decennio fa. Gli Stati Uniti avevano già effettuato la loro commercializzazione di NMN prima del 1994 sulla base dell'annuncio della FDA. Il governo giapponese del Ministero della Salute, del Lavoro e del Welfare ha rilasciato una decisione sul NMN come ingrediente alimentare nel 2019. E nel 2023, la Commissione sanitaria nazionale cinese accetta pubblicamenteProposteper NMN come additivo alimentare.
SupervisionePolitica per NMN in Giappone

Figura 1
Il governo del Ministero della Salute, del Lavoro e del Welfare ha rilasciato le relative politiche che non vi è alcun elemento soddisfa ilCriteri di giudizioed è intrinsecamente presente nel cibo (contenuto nel).Si è ritenuto opportuno affermare che i NMN non sono etichettati come aventi l'efficacia di un medicinale e che non si presume che siano ingredienti medicinali.( Figura 1)
Vale a dire,NMN è regolamentato come ingrediente alimentare in Giappone.Secondo la legge giapponese correlata, NMN può essere venduto come integratore alimentare, ma non può essere commercializzato per specifici benefici per la salute. NMN non è un farmaco farmaceutico e non richiede l'approvazione del governo giapponese prima di poter essere venduto. Tuttavia, i produttori di prodotti NMN devono garantire che i loro prodotti soddisfino i requisiti di sicurezza e di etichettatura e che qualsiasi affermazione fatta sul prodotto sia accurata e non fuorviante.
Politica di supervisione per NMN in Cina
All'inizio del 2022, la China National Medical Product Administration ha annunciato l'approvazione del deposito di NMN come nuovo ingrediente cosmetico, il che significa che è legale per le aziende cosmetiche in Cina che hanno completato con successo il deposito incorporare NMN nella produzione di cosmetici, mentre altre aziende che non hanno effettuato il deposito possono utilizzare NMN nei loro cosmetici dopo un periodo di protezione di tre anni.( Figura 2)

Figura 2
NMN è considerato un nuovo ingrediente alimentare e non è ancora approvato per l'uso come integratore alimentare. Tuttavia, il 28 gennaio 2023, la Commissione sanitaria nazionale cinese ha pubblicato pubblicamente un avviso sull'accettazione di nuove varietà di additivi alimentari, indicando che la domanda di NMN come additivo alimentare aveva iniziato ad essere accettata.( Figura 3)

Figura 3
Ma le aziende che producono NMN in Cina sono autorizzate a stabilire attività di esportazione e il produttore di materie prime NMN dovrebbe garantire che i loro prodotti soddisfino i relativi standard di esportazione per obbedire agli articoli di legge corrispondenti.
Politica di supervisione per NMN in America
La FDA (Food and Drug Adminitration) classifica NMN come integratore alimentare e lo regola ai sensi del Dietary Supplement Health and Education Act (DSHEA) di 1994. Sotto DSHEA, i produttori di integratori alimentari sono responsabili di garantire la sicurezza e l'etichettatura dei loro prodotti, ma la FDA non esamina o approva questi prodotti prima che raggiungano il mercato.
D'altra parte, molte aziende di materie prime NMN che vendono NMN possono fare affermazioni auto-affermate, ma queste affermazioni non sono esaminate o approvate dalla FDA. Quindi, quando si tratta di NMN come integratori alimentari, la preoccupazione dei consumatori per NMN potrebbe non essere stata accuratamente testata e può avere effetti collaterali inaspettati.
Ancora più importante, nell'ottobre 2022, sulla lettera di risposta a una società cinese che presenta la domanda per l'NDI (nuovi ingredienti dietetici) di NMN, la FDA ha affrontato che NMN è escluso dalla definizione di integratore alimentare sotto l'articolo della FDA ha autorizzato NMN per la ricerca come nuovo farmaco e potrebbe non essere commercializzata come o in un integratore alimentare.
Politica di supervisione per NMN in Australia

Figura 4
In Australia, la Therapeutic Goods Administration (TGA) è l'agenzia responsabile della regolamentazione dei beni terapeutici, compresi gli integratori alimentari.Gli integratori contenenti NMN sono considerati un tipo di medicina complementare e sono soggetti alla supervisione e alla regolamentazione di TGA.Il TGA richiede che qualsiasi affermazione fatta sui benefici di un prodotto sia supportata da prove e sia inclusa sull'etichetta del prodotto. La TGA ha anche il potere di agire contro le aziende che fanno affermazioni false o fuorvianti sui loro prodotti.( Figura 4)

Figura 5
SpecificamenteTGA ha dimostrato l'efficacia di NMN nel mantenere il livello di energia, produzione di energia, funzione del sistema nervoso, salute del sistema nervoso, salute della pelle, salute delle mucose del corpo salute generale e benessere e così via.( Figura 5)
Politica di supervisione per NMN in Canada

Grafico 6
In Canada,NMN è considerato un prodotto per la salute naturale ed è regolato come tale da Health Canada.Per essere venduto come prodotto per la salute naturale, NMN deve soddisfare determinati requisiti, come avere una licenza ed essere prodotto in conformità con le buone pratiche di fabbricazione (GMP). Inoltre,C'è un caso reale dimostrato sul sito ufficiale che i prodotti NMN hanno ottenuto il numero NPN per commercializzare prodotti correlati.(Figura 6)
Tuttavia, la preoccupazione principale in Canada è che la sicurezza e l'efficacia di NMN come prodotto sanitario non sono state ampiamente studiate e ci sono prove scientifiche limitate a sostegno del suo uso per anti-invecchiamento o altri benefici per la salute.
Referenze:
//www.mhlw.go.jp/stf/newpage_07867.html
//www.tga.gov.au/resources/artg/390600
//www.canada.ca/en/health-canada/services/drugs-health-products/natural-non-prescription.html
//ods.od.nih.gov/About/DSHEA_Wording.aspx