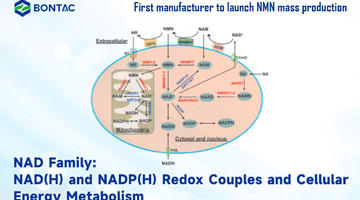
Le ultime ricerche dimostrano: il coenzima NAD+ può migliorare l'immunità tumorale! Commento dell'esperto dell'Accademia cinese delle scienze
Il 10 agosto 2021, i ricercatori dell'Università della Scienza e della Tecnologia di Shanghai hanno pubblicato un articolo intitolato L'integratore NAD + potenzia la funzione di uccisione del tumore salvando la trascrizione NAMPT TUBBY-mediata difettosa nelle cellule T infiltrate dal tumore in Cell Reports, rivelando che NAD + in integrato durante la terapia CAR-T e la terapia con inibitori del checkpoint immunitario, può migliorare l'attività antitumorale di T.
.jpg)
Attualmente, il precursore supplementare del NAD+, come prodotto nutrizionale, è stato verificato per la sicurezza del consumo umano. Questo risultato fornisce un nuovo metodo semplice e fattibile per migliorare l'attività antitumorale delle cellule T.
Le immunoterapie antitumorali, incluso il trasferimento adottivo di linfociti infiltranti il tumore (TIL) naturali e cellule T geneticamente modificate, nonché l'uso del blocco del checkpoint immunitario (ICB) per aumentare la funzione delle cellule T, sono emersi come approcci promettenti per ottenere risposte cliniche durature di tumori altrimenti refrattari al trattamento (Lee et al., 2015; Rosenberg e Restifo, 2015; Sharma e Allison, 2015). Sebbene le immunoterapie siano state utilizzate con successo in clinica, il numero di pazienti che ne beneficiano è ancora limitato (Fradet et al., 2019; Newick et al., 2017). L'immunosoppressione correlata al microambiente tumorale (TME) è emersa come la ragione principale per una risposta bassa e/o assente a entrambe le immunoterapie (Ninomiya et al., 2015; Schoenfeld e Hellmann, 2020). Pertanto, gli sforzi per studiare e superare i limiti legati alla TME nelle terapie immunitarie sono di grande urgenza.
.jpg)
Il fatto che le cellule immunitarie e le cellule tumorali condividano molte vie metaboliche fondamentali implica una competizione inconciliabile per i nutrienti nella TME (Andrejeva e Rathmell, 2017; Chang et al., 2015). Durante la proliferazione incontrollata, le cellule tumorali dirottano percorsi alternativi per una generazione più rapida di metaboliti (Vander Heiden et al., 2009). Di conseguenza, l'esaurimento dei nutrienti, l'ipossia, l'acidità e la generazione di metaboliti che possono essere tossici nella TME possono ostacolare il successo dell'immunoterapia (Weinberg et al., 2010). Infatti, i TIL spesso sperimentano stress mitocondriale all'interno dei tumori in crescita e si esauriscono (Scharping et al., 2016). È interessante notare che diversi studi indicano anche che i cambiamenti metabolici nella TME potrebbero rimodellare la differenziazione delle cellule T e l'attività funzionale (Bailis et al., 2019; Chang et al., 2013; Peng et al., 2016). Tutte queste evidenze ci hanno ispirato a ipotizzare che la riprogrammazione metabolica nelle cellule T potrebbe salvarle da un ambiente metabolico stressato, rinvigorendo così la loro attività antitumorale (Buck et al., 2016; Zhang et al., 2017).
In questo studio, integrando sia gli schermi genetici che chimici, abbiamo identificato che NAMPT, un gene chiave coinvolto nella biosintesi di NAD +, era essenziale per l'attivazione delle cellule T. L'inibizione di NAMPT ha portato a un robusto declino del NAD + nelle cellule T, interrompendo così la regolazione della glicolisi e la funzione mitocondriale, bloccando la sintesi di ATP e smorzando la cascata di segnalazione a valle del recettore delle cellule T (TCR). Basandoci sull'osservazione che i TIL hanno livelli di espressione di NAD + e NAMPT relativamente più bassi rispetto alle cellule T delle cellule mononucleate del sangue periferico (PBMC) nelle pazienti con cancro ovarico, abbiamo eseguito lo screening genetico nelle cellule T e identificato che Tubby (TUB) è un fattore di trascrizione per NAMPT. Infine, abbiamo applicato questa conoscenza di base nella (pre) clinica e abbiamo mostrato prove molto forti che l'integrazione con NAD + migliora notevolmente l'attività di uccisione antitumorale sia nella terapia con cellule CAR-T trasferite adottivamente che nella terapia di blocco del punto di controllo immunitario, indicando il loro promettente potenziale per il metabolismo di NAD + per trattare meglio i tumori.
1.NAD+ regola l'attivazione delle cellule T influenzando il metabolismo energetico
Dopo la stimolazione dell'antigene, le cellule T subiscono una riprogrammazione metabolica, dall'ossidazione mitocondriale alla glicolisi come principale fonte di ATP. Pur mantenendo sufficienti funzioni mitocondriali per supportare la proliferazione cellulare e le funzioni effettrici. Dato che NAD + è il principale coenzima per redox, i ricercatori hanno verificato l'effetto di NAD + sul livello del metabolismo nelle cellule T attraverso esperimenti come la spettrometria di massa metabolica e l'etichettatura isotopica. I risultati degli esperimenti in vitro mostrano che il deficit di NAD+ ridurrà significativamente il livello di glicolisi, il ciclo TCA e il metabolismo della catena di trasporto degli elettroni nelle cellule T. Attraverso l'esperimento di reintegro di ATP, i ricercatori hanno scoperto che la mancanza di NAD + inibisce principalmente la produzione di ATP nelle cellule T, riducendo così il livello di attivazione delle cellule T.
.jpg)
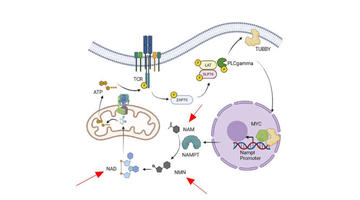
2.La via di sintesi di salvataggio NAD+ regolata da NAMPT è essenziale per l'attivazione delle cellule T
Il processo di riprogrammazione metabolica regola l'attivazione e la differenziazione delle cellule immunitarie. Il targeting del metabolismo delle cellule T offre l'opportunità di modulare la risposta immunitaria in modo cellulare. Anche le cellule immunitarie nel microambiente tumorale, il loro livello metabolico sarà influenzato corrispondentemente. I ricercatori in questo articolo hanno scoperto l'importante ruolo di NAMPT nell'attivazione delle cellule T attraverso lo screening dell'intero sgRNA del genoma e gli esperimenti di screening di inibitori di piccole molecole correlati al metabolismo. La nicotinammide adenina dinucleotide (NAD+) è un coenzima per le reazioni redox e può essere sintetizzata attraverso la via di salvataggio, la via di sintesi de novo e la via di Preiss-Handler. L'enzima metabolico NAMPT è principalmente coinvolto nella via di sintesi di salvataggio NAD+. L'analisi dei campioni tumorali clinici ha rilevato che nelle cellule T infiltranti il tumore, i loro livelli di NAD + e livelli di NAMPT erano inferiori rispetto ad altre cellule T. I ricercatori ipotizzano che i livelli di NAD + possano essere uno dei fattori che influenzano l'attività antitumorale delle cellule T infiltranti il tumore.
3.Supplemento NAD+ per migliorare l'attività antitumorale delle cellule T
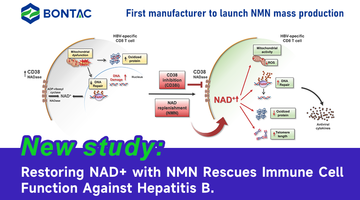
L'immunoterapia è stata una ricerca esplorativa nel trattamento del cancro, ma il problema principale è la migliore strategia di trattamento e l'efficacia dell'immunoterapia nella popolazione complessiva. I ricercatori vogliono studiare se migliorare la capacità di attivazione delle cellule T integrando i livelli di NAD + può migliorare l'effetto dell'immunoterapia basata sulle cellule T. Allo stesso tempo, nel modello di terapia CAR-T anti-CD19 e nel modello di terapia inibitore del checkpoint immunitario anti-PD-1, è stato verificato che l'integrazione di NAD + ha migliorato significativamente l'effetto di uccisione del tumore delle cellule T. I ricercatori hanno scoperto che nel modello di trattamento CAR-T anti-CD19, quasi tutti i topi nel gruppo di trattamento CAR-T integrati con NAD + hanno raggiunto la clearance tumorale, mentre il gruppo di trattamento CAR-T senza NAD + ha integrato solo circa il 20% dei topi ha raggiunto la clearance del tumore. Coerentemente con questo, nel modello di trattamento con inibitori del checkpoint immunitario anti-PD-1, i tumori B16F10 sono relativamente tolleranti al trattamento anti-PD-1 e l'effetto inibitorio non è significativo. Tuttavia, la crescita dei tumori B16F10 nel gruppo di trattamento anti-PD-1 e NAD + potrebbe essere significativamente inibita. Sulla base di questo, l'integrazione di NAD + può migliorare l'effetto antitumorale dell'immunoterapia basata sulle cellule T.
.jpg)
4.Come integrare NAD+
La molecola NAD+ è grande e non può essere direttamente assorbita e utilizzata dal corpo umano. Il NAD + ingerito direttamente per via orale è principalmente idrolizzato dalle cellule del bordo del pennello nell'intestino tenue. In termini di pensiero, c'è davvero un altro modo per integrare NAD +, che è quello di trovare un modo per integrare una certa sostanza in modo che possa sintetizzare NAD + autonomamente nel corpo umano. Esistono tre modi per sintetizzare NAD+ nel corpo umano: via di Preiss-Handler, via di sintesi de novo e via di sintesi di salvataggio. Sebbene i tre modi possano sintetizzare NAD +, c'è anche una distinzione primaria e secondaria. Tra questi, il NAD+ prodotto dalle prime due vie sintetiche rappresenta solo circa il 15% del totale del NAD+ umano e il restante 85% è raggiunto attraverso la via della sintesi correttiva. In altre parole, il percorso di sintesi di salvataggio è la chiave per il corpo umano per integrare NAD +.
Tra i precursori del NAD+, la nicotinamide (NAM), la NMN e la nicotinammide ribosio (NR) sintetizzano tutte NAD+ attraverso una via di sintesi di salvataggio, quindi queste tre sostanze sono diventate la scelta del corpo per integrare NAD+.
Sebbene NR in sé non abbia effetti collaterali, nel processo di sintesi di NAD +, la maggior parte di esso non viene convertito direttamente in NMN, ma deve essere prima digerito in NAM e quindi partecipare alla sintesi di NMN, che ancora non può sfuggire alla limitazione degli enzimi limitanti la velocità. Pertanto, anche la capacità di integrare NAD+ attraverso la somministrazione orale di NR è limitata.
Come precursore per l'integrazione di NAD +, NMN non solo bypassa la restrizione degli enzimi limitanti, ma viene anche assorbito molto rapidamente nel corpo e può essere convertito direttamente in NAD +. Pertanto, può essere utilizzato come metodo diretto, rapido ed efficace per integrare NAD +.
Recensioni degli esperti:
Xu Chenqi (Centro di eccellenza e innovazione della scienza cellulare molecolare, Accademia cinese delle scienze, esperto di ricerca in immunologia)
Il trattamento del cancro è un problema nel mondo. Lo sviluppo dell'immunoterapia ha compensato i limiti del trattamento tradizionale del cancro e ha ampliato i metodi di trattamento dei medici. L'immunoterapia del cancro può essere suddivisa in terapia di blocco del checkpoint immunitario, terapia con cellule T ingegnerizzate, vaccino tumorale, ecc. Questi metodi di trattamento hanno svolto un certo ruolo nel trattamento clinico del cancro. Allo stesso tempo, questo rende anche l'attuale focus della ricerca sull'immunoterapia su come migliorare ulteriormente l'effetto dell'immunoterapia ed espandere i benefici dell'immunoterapia.